|
|
|
Наблюдаемое в последние годы в большинстве развитых стран мира постарение населения сопровождается увеличением количества клапанных пороков сердца, связанных с возрастом и кальцинозом клапанов. Причем кальцинирующие поражения сердца стремятся занять лидирующее положение среди заболеваний у пожилых.
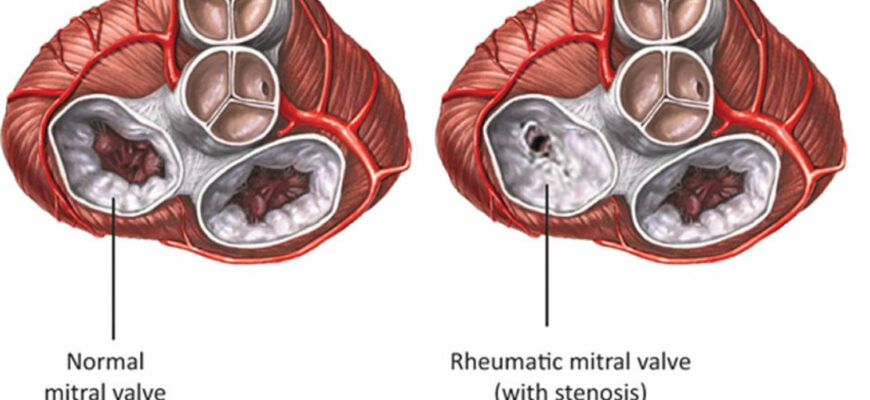
Как определить кальцинированный стеноз аортального клапана?Кальцинированный стеноз аортального клапана– это возрастной дегенеративный кальциноз преимущественно клапана аорты с формированием его стеноза.
Одни авторы предпочитают называть не воспалительный кальцинированный стеноз атеросклеротическим, другие – «пороком Менкенберга» или «менкерберговским типом обызвествления», третьи – «сенильный стеноз устья аорты». Большинство же авторов используют термин дегенеративный кальцинированный стеноз. Часто кальцинированный АС сочетается с кальцинозом минтального клапана, межжелудочковой перегородки, пучка Гиса и его ножек.
Происхождение
Гипотеза «wear and tear» – возрастного изнашивания, склерозирования и пассивной кальцификации аортального клапана в последние годы претерпела существенные изменения. Кальцификация – это не просто отложение кристаллов кальция фосфата, а организованный регулируемый процесс во многом сходный с формированием костной ткани, возможно детерминированный генами, отвечающими за регуляцию минерального обмена.
Нет оснований объяснять кальцификацию аортального клапана как проявление естественного процесса старения. Некоторые авторы считают кальцинированный АС одним из финальных проявлений атеросклероза, опираясь на общие для них факторы риска (возраст, пол, курение, артериальная гипертензия, сахарный диабет).
Другие не нашли связи между общепринятыми факторами риска и кальцинированным АС, но обнаружили причинно-следственную связь между остеопорозом и кальцификацией клапанов. По данным этих авторов, кальцификации и стенозированию аортального клапана способствует возраст, остеопороз, атерогенная дислипидемия, нарушение равновесия между синтезом и разрушением внеклеточного матрикса, почечная недостаточность и воспалительные изменения.
Патогенез
Ведущим звеном патогенеза кальцинированного АС в настоящее время рассматривают генетически детерминированное аутоиммунное воспаление, вызывающее дисбаланс между образованием и разрушением внеклеточного матрикса и способствующее формированию обструкции на уровне клапанов.
Вначале выявляют липоидную инфильтрацию фиброзного и субэндотелиального слоев полулунных заслонок. Возникновение липоидоза рассматривают как пред стадию кальциноза, возникающую в ответ на дегенерацию ткани. Деструкция этих участков сопровождается накоплением в них известковых отложений. В результате их разлома происходит набухание и петрификация белковых масс.
Поверхность клапана становится неровной, бугристой, утолщенной, полулуния утрачивают подвижность, но без сращения комиссур. Кальциноз может развиваться и без участия липидов – вследствие изменения физико-химических свойств крови и ткани. Кальцинаты могут формироваться и на мембранозной части межжелудочковой перегородки, захватывать проводящую систему сердца и стать источником серьезных аритмий.
Как проявляется болезнь?
Длительное время АС остаётся компенсированным заболеванием.Первыми симптомами, с которыми пациенты обращаются к врачу, являются головокружение, приступы слабости, загрудинные боли и перебои в работе сердца.
При прогрессировании появляется триада симптомов: синкопы, боли стенокардитического характера и одышка при развитии сердечной недостаточности. Синкопы в основном наблюдаются при физической нагрузке. Они могут быть следствием недостаточного прироста сердечного выброса из-за обструкции выходного тракта левого желудочка, в результате чего уменьшается системное артериальное давление и мозговая перфузия. Помимо того повышение давления в левом желудочке при нагрузке может инициировать системную вазопрессорную реакцию и снижать системное АД, что в свою очередь порождает синкопальное состояние.
Стенокардия по сути обусловлена преимущественно изменениями гемодинамики. С одной стороны появление боли за грудиной связано с турбуленцией крови над кальцинированным клапаном около устья коронарного синуса и недостаточным поступлением ее в коронарное русло. С другой стороны развивающая при этом пороке гипертрофия левого желудочка значительно повышает потребность миокарда в кислороде. При аускультации выслушивается классический систолический шум изгнания в проекции аортального клапана. Шум проводится на сосуды шеи. Учитывая, что при кальцинированном АС поток крови проходит через суженное отверстие, но с подвижными створками, которые гасят низкочастотные компоненты шума, он может иметь мягкий тембр и напоминать «крик чайки». Шум может проводиться на верхушку сердца, и иногда он воспринимается как шум митральной регургитации. Это так называемый феномен Галлавердена.
Интенсивность систолического шума при кальцинированном АС увеличивается во время приседания и уменьшается при пробе Вальсальвы или в вертикальном положении. Может отмечаться ослабление аортального компонента II тона. Частым проявлением кальцинированного АС может быть пролабирование клапана. Пролапс митрального или аортального клапана появившийся в пожилом возрасте должен предполагать наличие кальциноза.
У больных с кальцинированным АС часто развиваются нарушения ритма, имеющие серьезную прогностическую значимость. У 28% пациентов отмечали эпизоды пароксизмальнойфибрилляции предсердий, у 26% – постоянную форму фибрилляции предсердий. У 14% больных с АС наблюдали различные варианты атриовентрикулярных блокад. Более двух третей пациентов нуждаются в имплантации искусственного водителя ритма.
Достаточную проблему у этих больных представляет профилактика тромбоэмболических осложнений. С одной стороны, отложение кальцинатов на створках клапанов могут иметь самостоятельное значение в развитии эмболических осложнений и инициировать инсульты, инфаркты миокарда и окклюзии периферических артерий, что требует профилактического применения антикоагулянтов.
С другой, постоянная травматизация тромбоцитов на кальцинированных створках может способствовать предрасположенности к кровотечениям. По мере присоединения симптомов снижается показатель выживаемости, так при появлении стенокардии продолжительность жизни сокращается до 5 лет, при присоединении синкопов до 3 лет, а при развитии сердечной недостаточности до 2 лет. Внезапно умирают 10% больных со стенокардией, 15% – с синкопами и 25% при сердечной недостаточности.
|
|
|
Диагностика
Эхокардиография рассматривается в качестве ключевого метода диагностики кальцинированного АС. Эхокардиография позволяет установить количество створок, оценить их движение, утолщение, наличие кальцинатов, определить степень стенозирования. Nightingale A.K., Horowitz J.D. выделили 3 степени кальциноза: 0-норма – включение кальция не выявляются, 1-я легкая степень – одиночные включения кальция на одной створке, 2-я средняя степень – одиночные включения на двух створках и массивное поражение одной створки, 3-я тяжелая степень – массивное поражение двух створок или одиночные включения на всех трех створках. Степень тяжести АС устанавливается с учетом площади аортального клапана, максимальной скорости тока крови, и градиента давления.
Как рекомендует последняя версия ESС /EACTS (2012) допплерэхокардиографические критерии тяжелого стеноза следующие: площадь клапана S< 1,0 см2, индекс площади < 0,6 см/м2, градиент давления ∆P > 40 мм рт. ст., максимальная скорость потока Vmax > 4 м/с. Площадь клапана S<0,8 см2 соответствует критическому стенозу.
Для выявления псевдостеноза рекомендуют использовать стресс-эхокардиографический тест с добутамином (прирост ударного объема >20% при введении добутамина в низких дозах). При истинном тяжелом АС увеличение скорости кровотока сопровождается увеличением градиента давления и незначительными изменениями площади (увеличение< 0,2 см2). В то время как при псевдостенозе отмечается значительное увеличение площади клапана при минимальном изменении градиента.
Какое лечение использовать?
Основным методом лечения кальцинированного АС является хирургическое лечение. Для тяжелого АС других методов не разработано. Согласно последней версии рекомендаций ESС /EACTS (2012) хирургическое лечение показано: симптомным пациентам с тяжелым АС (S<1 см2 или <0,6 см/м2, ∆P <40 мм рт. ст.); пациентам с тяжелым стенозом, подвергшихся аорто-коронарному шунтированию, хирургическому вмешательству на восходящем отделе аорты и/или других клапанах; асимптомным пациентам с тяжелым АС и фракцией выброса < 50%; асимптомным пациентам с тяжелым АС, у которых при выполнении теста с физической нагрузкой появляются симптомы, ассоциированные со стенозом.
Хирургическое лечение может быть также рекомендовано: пациентам с умеренным АС, подвергшихся аорто-коронарному шунтированию, оперативному вмешательству на восходящей части аорты или других клапанах; пациентам с низким хирургическим риском, нормальной реакцией на тест с физической нагрузкой и очень тяжелым АС (Vmax > 5,5 м/с) или комбинации тяжелой кальцификации клапана и ежегодным приростом Vmax > 0,3 м/с.
Летальность, ассоциированная с хирургическим вмешательством, составляет 4-8%. Факторы, повышающие риск смертности при оперативном вмешательстве: пожилой возраст, коморбидные состояния, женский пол, высокий функциональный класс больного, экстренные операции, дисфункция левого желудочка, легочная гипертензия, ИБС и предшествующие операции на клапанах. При этом следует отметить, что хирургическое лечение существенно увеличивает продолжительность и качество жизни пациентов старше 80 лет, поэтому пожилой возраст не является противопоказанием для этого вида терапии.Проблему представляют больные, которым невозможно выполнить хирургическую замену клапана из-за высокого операционного риска.
А это около 30% пациентов с тяжелыми симптоматическими формами АС, которым операция противопоказана в связи с преклонным возрастом, наличием дисфункции левого желудочка и сопутствующих заболеваний. У таких больных рассматривается возможность применения транскатетерной баллонной вальвулопластики.
Метод транскатетерной вальвулопластики аортального клапана представляет собой новую манипуляцию, во время которой биопротезный клапан вводится через катетер и имплантируется в пораженный нативный аортальный клапан. Однако с момента внедрения этой методики в клиническую практику, накопились данные, которые свидетельствуют, что данный метод является высокоэффективным только в педиатрии. Применение баллонной вальвулопластики у взрослых сопряжено с низкой эффективностью, с высоким риском осложнений (>10%) и рестенозов.
У 1-5% пациентов после данной процедуры развиваются инсульты, у 20% различные сосудистые осложнения, а 7-40% нуждаются в имплантации искусственного пейсмекера [11,18,19] Отдаленные результаты не демонстрируют преимуществ метода в сравнении с обычным течением АС. Метод транскатетерной баллонной вальвулопластики можно рассматривать как своеобразный переходный мостик при нестабильной гемодинамике у пациентов с тяжелым АС при необходимости не кардиологических хирургических вмешательств.
Абсолютные противопоказания для баллонной вальвулопластики: размер аортального отверстия< 18 мм или > 28 мм; тромб в левом желудочке; активный эндокардит; угроза развития кальциноза коронарного синуса (асимметричные кальцинаты на клапане, близкое к клапану расположение коронарного синуса). Относительные противопоказания для баллонной вальвулопластики: двустворчатый аортальный клапан; необходимость аорто-коронарного шунтирования; фракция выброса< 20%.Медикаментозное лечение для больных с кальцинированным АС не разработано. Пациенты, у которых заболевание протекает без симптомов, в лечении не нуждаются.
Симптомным пациентам необходимо вовремя рекомендовать хирургическое лечение. Тем пациентам, которые не могут быть прооперированы, рекомендуют назначать сердечные гликозиды, диуретики, ингибиторы ангиотензинпревращающего фермента (АПФ), или блокаторы рецепторов ангиотензина II (БРА II) при развитии у них сердечной недостаточности.
Ингибиторы АПФ существенно влияют на постнагрузку и преднагрузку и могут вызывать постуральные гипотензии. Применение ингибиторов АПФ при АС должно быть строго индивидуальным с тщательным титрованием доз от минимальных до максимально переносимых. На преднагрузку в меньшей степени оказывают влияние БРА II и при их использовании менее вероятно развитие постуральных явлений, поэтому применение БРА II при АС более желательно.
Помимо того БРА II существенно снижают массу миокарда при гипертрофии левого желудочка и способствуют улучшению диастолической функции. Кальцинированный АС активно прогрессирует подобно атеросклерозу. Предполагалось, что интенсивная терапия статинами должна замедлить процессы кальцинированного поражения аортального клапана. Эффект статинов в этой клинической ситуации не оправдался, назначение этих препаратов не замедляет прогрессирование кальцинированного АС.
Терапия статинами не рекомендуется для лечения изолированного кальцинированного АС, но с другой стороны назначение статинов может быть рекомендовано для модификации факторов риска и вторичной профилактики атеросклероза у этих же пациентов.
Факторы прогрессирования кальцинированного аортального стеноза можно разделить на модифицируемые и немодифицируемые. К модифицируемым относятся курение, мужской пол, гипергликемия, гиперкальциемия, ожирение и почечная недостаточность. К немодифицируемым – врожденный двустворчатый клапан и кальцификация митрального клапана . Наличие АГ непосредственно не влияет на прогрессирование АС, но значительно усложняет его клиническое течение.
Темпы прогрессирования хорошо отслеживаются по показателям допплерэхокардиографии. Пациентов с ежегодным приростом Vmax > 0,3 м/с и ∆P > 7 мм рт. ст. следует отнести в группу очень высокого риска и рассмотреть вопрос о безотлагательной хирургической коррекции порока.
Таким образом, кальцинированный АС достаточно распространенная в последнее время патология.
|
|
|